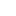像 AlphaFold 这样的蛋白质结构预测工具,已经帮助我们深入了解了蛋白质如何相互作用从而发挥其功能,但这些工具无法创建新的蛋白质来直接控制这些相互作用。
现在,Google DeepMind 团队推出了一种用于设计「与目标分子结合更紧密」的新型蛋白质的 AI 系统 AlphaProteo。
在测试的 7 种靶蛋白上,AlphaProteo 的实验成功率更高,在湿实验室中测试中,9% 到 88% 候选分子成功结合,这比其他方法高出 5 到 100 倍。而且,比现有最佳方法的结合亲和力高出 3 到 300 倍。

仅需一轮中等通量筛选且无需进一步优化,AlphaProteo 便可生成适用于多种应用的「即用型」结合剂。它可以帮助科学家更好地了解生物系统如何运作,节省研究时间,推进药物设计等等。
该团队于 2024 年 9 月 5 日上线了最新论文《De novo design of high-affinity protein binders with AlphaProteo》。

论文链接:https://storage.googleapis.com/deepmind-media/DeepMind.com/Blog/alphaproteo-generates-novel-proteins-for-biology-and-health-research/Protein_Design_White_Paper_2024.pdf
从细胞生长到免疫反应,身体中的每个生物过程都依赖于称为蛋白质的分子之间的相互作用。好比钥匙开锁一样,一种蛋白质可以与另一种蛋白质结合,帮助调节关键的细胞过程。
蛋白质-蛋白质相互作用是蛋白质功能的一个基本方面,蛋白质结合蛋白是治疗、诊断和生物医学研究的基本组成部分。
传统上,抗体、纳米抗体和其他支架(如 DARPins)通过免疫或定向进化开发成针对各种靶标的结合物。不过,实验选择无法控制目标表位,而且对于常规研究应用来说往往过于费力。
不使用天然蛋白质作为起点,从头计算设计结合物可以靶向预先指定的表位,并生成比抗体更小、更热稳定且更易于表达的结合物。
AlphaProteo 蛋白质设计系统
近期,基于深度学习的模型在生物分子结构预测和蛋白质设计方面取得了重大进展。这推动了关键科学和社会挑战的进展,包括蛋白质-蛋白质相互作用的预测和设计。
现在无需高通量筛选即可获得针对某些靶标的计算设计结合物。在某些情况下,无需进行实验优化即可实现高结合亲和力,例如对于小肽或无序靶标。
然而,针对凸表位或极性表位的成功率仍然很低,初始设计的亲和力通常很差,许多靶标仍然难以处理。
在最新的论文中,DeepMind 团队介绍了 AlphaProteo 蛋白质设计系统,并表明它可以设计从头蛋白质结合蛋白,该系统具有以下优势:
1、高成功率:通过筛选数十种设计候选物可以获得稳定、高表达和特异性的结合物,从而无需使用高通量方法。
2、高亲和力:对于除一个目标之外的每个测试目标,最佳结合剂具有亚纳摩尔或低纳摩尔结合亲和力(KD),从而最大限度地减少了下游亲和力优化所需的劳动力。
3、整体优势:使用单一设计方法,无需复杂的人工干预,即可成功获得针对一系列具有不同结构和生化特性的靶标的结合剂。
图示:AlphaProteo 概述。(来源:论文)
了解蛋白质相互结合的复杂方式
能够与靶蛋白紧密结合的蛋白质结合剂很难设计。传统方法耗时巨大,需要多轮大量的实验室工作。在创建结合剂后,它们还需要进行大量额外的实验从而优化结合亲和性。
AlphaProteo 经过蛋白质数据库 (PDB) 中的大量蛋白质数据和 AlphaFold 中的 1 亿多条预测结构的训练,已经了解了分子相互结合的无数方式。给定目标分子的结构和该分子上的一组首选结合位置,AlphaProteo 会生成一个候选蛋白质,该蛋白质在这些位置与目标结合。
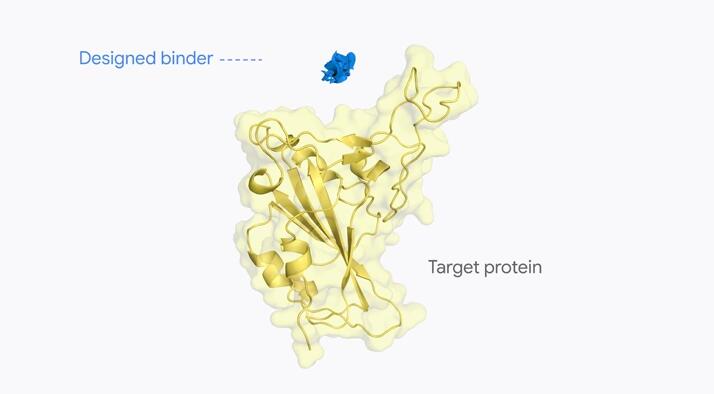
视频1:预测的蛋白质结合物结构与靶蛋白相互作用的图示。蓝色部分是 AlphaProteo 生成的预测蛋白质结合物结构,旨在与靶蛋白结合。黄色部分是靶蛋白,具体来说是 SARS-CoV-2 刺突受体结合域。(来源:DeepMind 官网)
在重要的蛋白质结合靶点上取得成功
为了测试 AlphaProteo,研究人员设计了针对各种靶蛋白的结合剂,包括两种与感染有关的病毒蛋白 BHRF1 和 SARS-CoV-2 刺突蛋白受体结合域 SC2RBD,以及五种与癌症、炎症和自身免疫性疾病有关的蛋白 IL-7Rɑ、PD-L1、TrkA、IL-17A 和 VEGF-A。
AlphaProteo 系统具有极具竞争力的结合成功率和一流的结合强度。对于七个靶点,AlphaProteo 在计算机模拟中生成候选蛋白,这些蛋白在实验测试时与目标蛋白紧密结合。
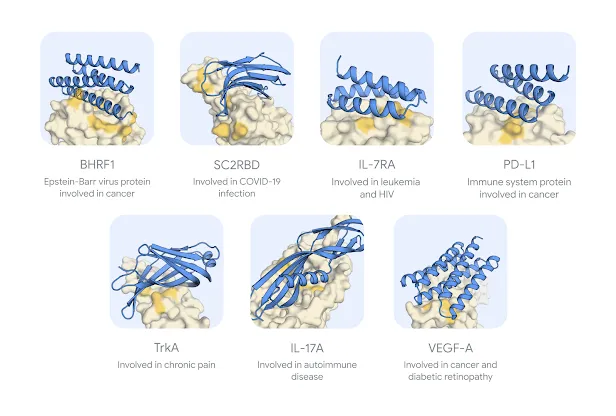
图示:AlphaProteo 为其生成成功结合剂的七种靶蛋白的预测结构图。蓝色表示在湿实验室中测试的结合剂示例,黄色是蛋白质靶点,深黄色突出显示的是预期的结合区域。(来源:论文)
对于一个特定靶标,即病毒蛋白 BHRF1,在 Google DeepMind Wet Lab 中进行测试时,88% 候选分子成功结合。根据测试的靶标,AlphaProteo 结合剂的结合力平均比现有最佳设计方法强 10 倍。
对于另一个靶标 TrkA,新结合剂甚至比经过多轮实验优化的针对该靶标的最佳先前设计结合剂更强。
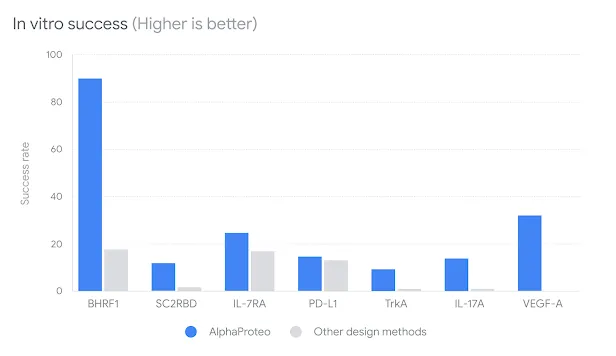
图示:与其他设计方法相比,AlphaProteo 针对七种目标蛋白的实验体外成功率。成功率越高,意味着需要测试的设计越少,才能找到成功的结合体。(来源:论文)
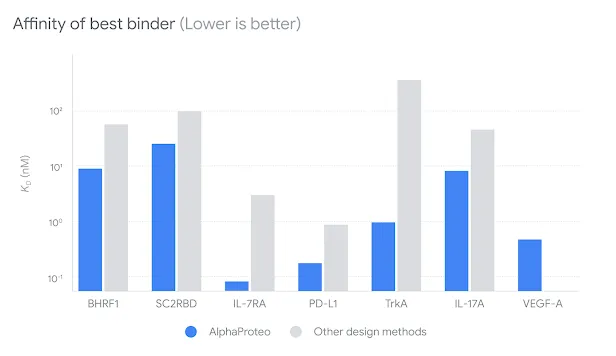
图示:与其他设计方法相比,AlphaProteo 的设计在未进行实验优化的情况下对七种目标蛋白的最佳亲和力。亲和力越低,意味着结合蛋白与目标蛋白的结合越紧密。(来源:论文)
对多种蛋白质的验证结果
研究人员除了在其湿实验室中进行计算机验证和测试 AlphaProteo 之外,还聘请了 Francis Crick 研究所的 Peter Cherepanov、Katie Bentley 和 David LV Bauer 研究小组来验证其蛋白质结合剂。
在不同的实验中,他们深入研究了一些更强的 SC2RBD 和 VEGF-A 结合剂。
研究小组证实,这些结合剂的结合相互作用确实与 AlphaProteo 所预测的相似。此外,研究小组还证实了这些结合剂具有有用的生物学功能。例如,一些 SC2RBD 结合剂被证明可以防止 SARS-CoV-2 及其某些变体感染细胞。
AlphaProteo 的性能表明,它可以大大减少涉及广泛应用的蛋白质结合剂的初始实验所需的时间。
然而,该人工智能系统有局限性,因为它无法针对第 8 个靶点 TNFɑ(一种与类风湿性关节炎等自身免疫性疾病相关的蛋白质)设计成功的结合物。研究人员选择 TNFɑ 来挑战 AlphaProteo,因为计算分析表明设计结合物非常困难。
接下来,该团队将继续改进和扩展 AlphaProteo 的功能,最终目标是解决这些具有挑战性的靶点。实现强结合通常只是设计可能对实际应用有用的蛋白质的第一步,在研发过程中还有更多的生物工程障碍需要克服。
开发更全面的蛋白质设计产品
蛋白质设计是一项快速发展的技术,在各个领域都具有巨大的科学进步潜力,从了解导致疾病的因素,到加速病毒爆发的诊断测试开发,支持更可持续的制造过程,甚至清除环境中的污染物。
未来,DeepMind 将与科学界合作,利用 AlphaProteo 解决有影响力的生物学问题并了解其局限性。他们还一直在 Isomorphic Labs 探索其药物设计应用,并对未来的发展感到兴奋。
该团队将不断提高 AlphaProteo 算法的成功率和亲和力,扩大它可以解决的设计问题范围,并与机器学习、结构生物学、生物化学和其他学科的研究人员合作,为社区开发负责任、更全面的蛋白质设计产品。
相信 AlphaProteo 将为许多生物应用开辟新的解决方案,例如控制细胞信号传导,成像蛋白质、细胞和组织,赋予各种效应系统目标特异性等等。